IOR 進口流程是什麼?為何需要了解?
IOR(Importer of Record,登記進口商)進口流程是指由 IOR 主體負責的完整進口作業流程,從下單採購、文件準備、報關申報到清關放行,每個環節都涉及法規合規與責任歸屬。根據 美國海關與邊境保護局(CBP)規定,IOR 必須確保所有進口商品符合美國聯邦法規要求,包含 FDA 食品法規、產品標籤與關稅申報等。
對台灣食品業者與跨境賣家而言,理解 IOR 進口流程的重要性在於:
- 釐清責任歸屬: 明確 IOR 與賣家在各環節的職責分工
- 避免清關延誤: 掌握文件準備時間點,減少扣關風險
- 降低合規成本: 提前規劃可避免補件、罰款等額外支出
- 提升物流效率: 了解流程瓶頸,優化供應鏈管理
若尚未建立對 FDA 食品註冊制度的整體理解,建議先從完整總覽入手,有助於後續判斷不同情境與執行差異。
👉 FDA 食品註冊完整指南|台灣食品出口美國必讀(2026 最新)
https://greenoo.tw/fda-food-registration/
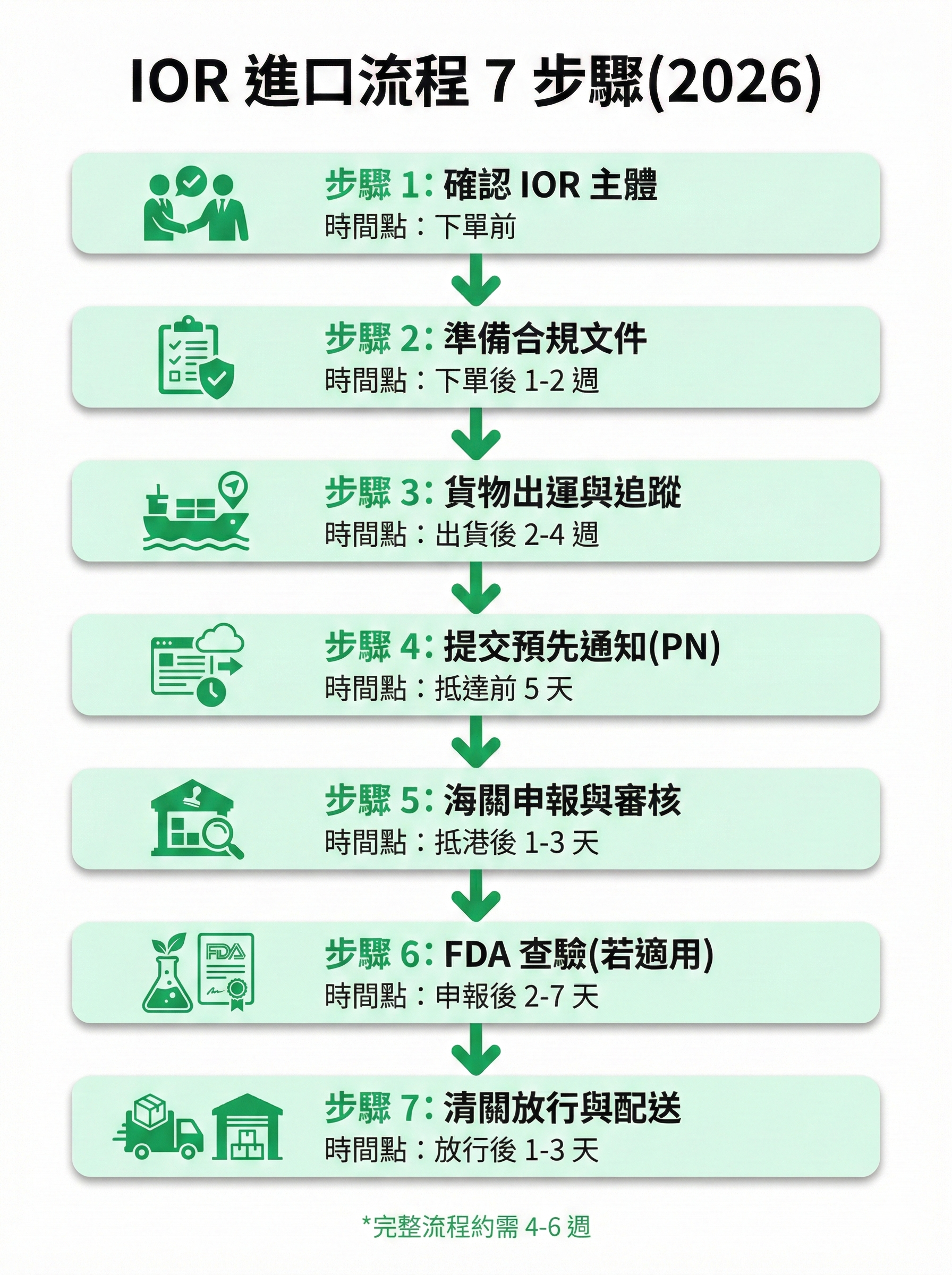
IOR 進口流程完整 7 步驟
步驟 1: 確認 IOR 主體與合約簽署(下單前)
在下單採購前,必須先確認誰擔任 IOR 角色。根據 CBP 進口商責任指南,IOR 可以是:
- 美國境內公司(最常見,如進口商、經銷商)
- 第三方 IOR 服務商(專業代理公司)
- 台灣賣家的美國子公司(若有設立)
必須完成的文件:
- IOR 服務合約(明確責任範圍、費用結構)
- 授權書(POA, Power of Attorney,授權報關行代為申報)
- 保險與擔保文件(Bond,用於關稅擔保)
Common Errors: 誤以為物流公司或貨代自動擔任 IOR,導致清關時責任不明。
步驟 2: 準備產品合規文件(下單後 1-2 週)
確認 IOR 後,需準備產品進口所需的合規文件。對食品類產品而言,根據 FDA 進口程序指南,必備文件包含:
| Document Type | Description | responsible party |
|---|---|---|
| FDA 食品設施註冊編號(FFR) | 證明製造工廠已註冊 | 台灣工廠/IOR |
| 預先通知(PN, Prior Notice) | 貨物抵達前提交 | IOR/報關行 |
| 產品標籤與成分表 | 符合 FDA 標籤規範 | Taiwan Seller |
| 檢驗報告(若適用) | 農藥殘留、微生物檢測等 | 台灣工廠 |
| 商業發票(Commercial Invoice) | 載明貨物價值、數量 | Taiwan Seller |
實務技巧: 建議在生產階段即同步準備文件,避免出貨後才發現缺件。
圖 2: IOR 進口流程完整步驟圖
步驟 3: 貨物出運與物流追蹤(出貨後 2-4 週)
貨物從台灣出運後,IOR 與賣家需共同追蹤物流狀態,確保文件與實際貨物資訊一致。
關鍵檢查點:
- 提單(Bill of Lading, B/L)資訊正確性
- 貨櫃封條號碼(Seal Number)與申報一致
- 預計抵達時間(ETA)更新
Frequently Asked Questions: 提單上的收貨人(Consignee)必須與 IOR 一致,否則海關可能拒絕放行。
步驟 4: 提交預先通知(PN, Prior Notice)(抵達前 5 天)
According to FDA 預先通知規定,所有食品類產品必須在抵達美國前提交 PN,內容包含:
- 產品名稱、成分、數量
- 製造商與 FDA 設施註冊編號(FFR)
- 預計抵達港口與時間
- IOR 與收貨人資訊
Submission Time Requirement:
- 海運: 抵達前不少於 8 小時
- 空運: 抵達前不少於 4 小時
- 陸運: 抵達前不少於 2 小時
Practical Recommendations: 由專業報關行或 IOR 服務商提交,避免格式錯誤導致扣關。
步驟 5: 海關申報與審核(抵港後 1-3 天)
貨物抵達美國港口後,報關行代表 IOR 向 CBP 提交正式進口申報(Entry Filing),包含:
- 商業發票(Commercial Invoice)
- 裝箱單(Packing List)
- 提單(Bill of Lading)
- FDA PN 確認號碼
審核流程:
- CBP 系統初步審核(自動化)
- 風險評估(可能觸發人工查驗)
- 關稅計算與繳納
扣關風險因素:
- 產品標籤不符 FDA 規範
- PN 資訊與實際貨物不符
- 列入 FDA 進口警示清單
步驟 6: FDA 查驗(若適用)(申報後 2-7 天)
若 CBP 或 FDA 判定需進一步查驗,貨物將被扣留進行檢驗。根據 FDA 進口查驗程序,查驗類型包含:
| 查驗類型 | Description | Processing Time |
|---|---|---|
| 文件審查(Document Review) | 僅檢查文件完整性 | 1-2 天 |
| 實體檢查(Physical Examination) | 開箱檢查產品外觀與標籤 | 3-5 days |
| 實驗室檢測(Lab Analysis) | 抽樣送檢(微生物、農藥等) | 7-14 天 |
應對策略:
- 主動提供補充文件(如檢驗報告)
- 若不符規定,可選擇退運或銷毀
- 嚴重違規可能列入進口警示,影響後續出貨
若進一步關心 FDA 食品註冊的扣關、查驗與常見錯誤,可參考以下說明頁面,以釐清實務上的判斷重點。
👉 FDA 食品註冊風險解析|扣關、查驗與常見錯誤整理(2026)
https://greenoo.tw/fda-food-registration-fda-food-registration-risks-and-inspections/
步驟 7: 清關放行與最後一哩配送(放行後 1-3 天)
通過所有審核後,CBP 發出放行通知(Release),貨物可正式進入美國市場。
放行後流程:
- IOR 繳納關稅與相關費用
- 貨物從港口提領
- 轉運至最終目的地(倉庫或 FBA)
費用結構(參考):
- 關稅(Duty): 依產品 HS Code 計算
- 港口雜費(Port Fees): 約 $50-150
- 報關行服務費: 約 $100-300
- IOR 服務費: 依合約而定
圖 3: IOR 進口流程常見問題檢核表
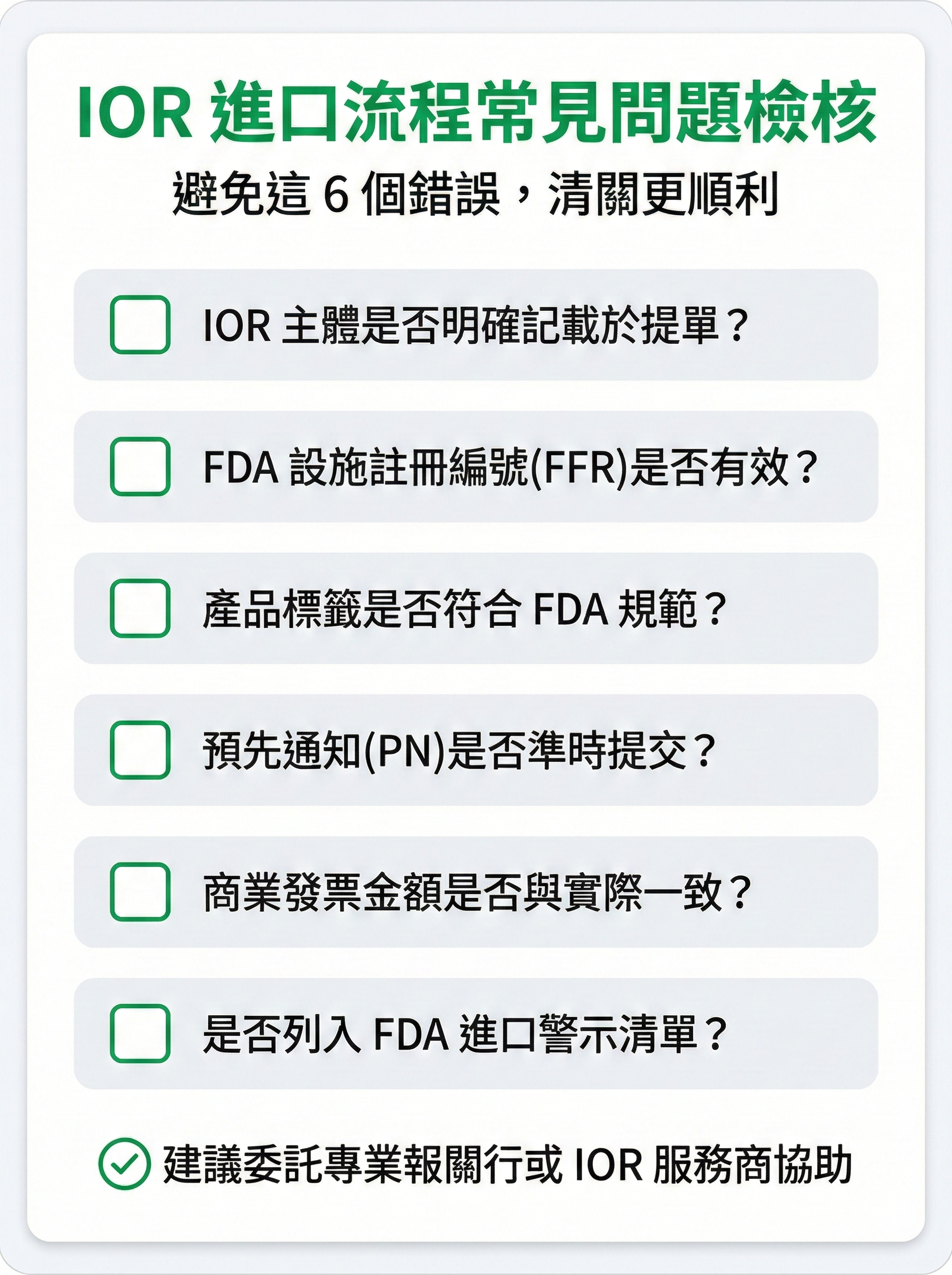
需要特別注意的 3 個實務重點
1. IOR 與賣家的責任分界
許多台灣賣家誤以為委託 IOR 後就不需負責,但實際上:
- 產品合規責任: 賣家仍需確保產品符合 FDA 規範(如標籤、成分)
- 文件提供責任: 賣家需提供正確的商業發票、產品資訊
- 後續責任: 若產品被召回或違規,賣家可能連帶受影響
⚠️ important reminder: IOR 服務合約應明確載明雙方責任範圍,避免糾紛。
2. FDA 預先通知(PN)的常見錯誤
- 錯誤 1: 產品名稱使用中文或不明確的英文(應使用 FDA 認可的通用名稱)
- 錯誤 2: FFR 編號填寫錯誤或過期
- 錯誤 3: 未更新預計抵達時間(ETA),導致 PN 失效
💡 實務技巧: 建議使用專業報關系統或委託報關行提交,系統會自動檢查格式錯誤。
3. 清關時間的不確定性
即使文件齊全,清關時間仍可能因以下因素延長:
- 港口擁塞(旺季如 11-12 月)
- 隨機抽檢(FDA 或 CBP)
- 新產品首次進口(審核較嚴格)
應對策略: 預留 1-2 週緩衝時間,避免影響銷售計畫。
若進一步關心 FDA 食品註冊的申請流程與所需文件,可參考以下說明頁面,以釐清實務上的判斷重點。
👉 FDA 食品註冊流程與文件完整說明|台灣申請重點整理(2026)
https://greenoo.tw/fda-food-registration-fda-food-registration-process-and-documents-taiwan/
Conclusion
IOR 進口流程從下單到清關涉及 7 個關鍵步驟,每個環節都需台灣賣家與 IOR 緊密配合:
- 步驟 1-2: 確認 IOR 主體與準備合規文件(下單前後)
- 步驟 3-4: 貨物出運與提交預先通知(出貨後 2-4 週)
- 步驟 5-7: 海關申報、FDA 查驗與清關放行(抵港後 1-2 週)
掌握完整流程有助於:
- 降低扣關風險
- 縮短清關時間
- 避免額外成本
- 提升供應鏈效率
若對 FDA 食品合規或 IOR 進口流程仍有疑問,歡迎參考 Green Circle Official Website 的專業顧問服務。
參考資料
本文內容基於以下官方資料撰寫(截至 2026 年 1 月):
- U.S. Customs and Border Protection. “Importer Responsibilities.” CBP.gov, https://www.cbp.gov/trade/basic-import-export/importer-responsibilities
- U.S. Food and Drug Administration. “Overview of the Importing Process for Foods.” FDA.gov, https://www.fda.gov/food/importing-food-products-united-states/overview-importing-process-foods
- U.S. Food and Drug Administration. “Prior Notice of Imported Food.” FDA.gov, https://www.fda.gov/food/importing-food-products-united-states/prior-notice-imported-food
- U.S. Food and Drug Administration. “Examination and Sampling of Imported Food.” FDA.gov, https://www.fda.gov/food/importing-food-products-united-states/examination-and-sampling-imported-food
註: 美國進口法規可能更新,建議查閱最新官方文件或諮詢專業顧問。