FDA 檢查報告是什麼?為何台灣業者需要了解?
According to FDA 檢查程序官方指南{:target=”_blank”},當 FDA 對食品設施進行現場檢查後,會根據發現的缺失嚴重程度,發出不同類型的檢查報告。台灣食品業者若出口美國,必須理解這三種報告的差異與應對方式:
- 483 表格(Form 483):列出檢查中發現的「可觀察到的缺失」,屬於初步通知
- EIR(Establishment Inspection Report):完整的檢查報告,記錄所有檢查細節
- 警告信(Warning Letter):正式的法規違規通知,要求立即改善
這三種文件的嚴重程度與法律效力完全不同,錯誤理解可能導致應對失當,甚至面臨進口扣留或法律訴訟The
為何 FDA 會進行食品設施檢查?
FDA 依據 FSMA(食品安全現代化法案){:target=”_blank”} 賦予的權力,對國內外食品設施進行定期或不定期檢查,目的包括:
- 驗證 FSMA 合規性:確認設施是否建立預防性控制計畫
- 調查食品安全事件:當發生污染或疾病爆發時追查源頭
- 例行性檢查:依風險等級定期檢查設施
- 進口產品驗證:針對進口食品的境外設施檢查
若尚未建立對 FDA 食品註冊制度的整體理解,建議先從完整總覽入手,有助於後續判斷不同情境與執行差異。
👉 FDA 食品註冊完整指南|台灣食品出口美國必讀(2026 最新)
https://greenoo.tw/fda-food-registration/
圖 2: FDA 檢查報告類型比較圖

483 表格(Form 483):可觀察到的缺失清單
什麼是 483 表格?
rely on FDA 檢查操作手冊(IOM){:target=”_blank”},483 表格是 FDA 檢查官在檢查結束時,向設施管理層當場發出的書面文件,列出檢查期間「可觀察到的缺失」(Objectionable Conditions)。
核心特性:
- 即時性:檢查結束當天發出,管理層需當場簽收
- 描述性:僅描述發現的缺失,不包含法律判定或處罰
- 初步性:並非最終結論,FDA 仍需進一步評估
483 表格的常見缺失類型
| 缺失類別 | 具體範例 | 嚴重程度 |
|---|---|---|
| 文件記錄不完整 | 食品安全計畫未更新、HACCP 記錄缺漏 | 低-中 |
| 衛生條件不佳 | 設備清潔不足、人員衛生管理缺失 | center |
| 製程控制問題 | 溫度監控不當、交叉污染風險 | 中-高 |
| Labeling irregularities | 過敏原標示錯誤、營養標示不完整 | center |
收到 483 表格後該如何應對?
建議回應時間:15 個工作天內(非強制,但 FDA 期待)
正確應對步驟:
- 立即內部檢討:召集相關部門確認缺失真實性
- 制定改善計畫:針對每項缺失提出具體改善措施
- 書面回覆 FDA:說明改善行動、完成時間與預防措施
- Keeping complete records:所有改善證據需留存備查
⚠️ important reminder:即使 483 表格不是正式處罰,若未妥善回應,FDA 可能升級為警告信或進口扣留。
EIR(Establishment Inspection Report):完整檢查報告
什麼是 EIR?
EIR 是 FDA 檢查官完成檢查後,提交給 FDA 總部的內部報告,記錄檢查的完整過程、發現的所有問題與檢查官的評估意見。
核心特性:
- 內部文件:主要供 FDA 內部使用,不會主動發給設施
- 全面性:包含檢查時間、範圍、發現問題、樣品採集等所有細節
- 分類依據:FDA 依據 EIR 內容,決定是否發出警告信或採取其他行動
EIR 的三種分類
rely on CFR Title 21 § 20.64{:target=”_blank”},EIR 分為三種分類:
- NAI(No Action Indicated):無需採取行動,設施合規
- VAI(Voluntary Action Indicated):建議自願改善,但無強制要求
- OAI(Official Action Indicated):需採取正式行動,可能發警告信或扣留產品
台灣業者能否取得 EIR?
可以,但需透過 FOIA(資訊自由法)申請:
- 申請網址:https://www.fda.gov/regulatory-information/freedom-information
- 處理時間:通常需 20-60 個工作天
- 費用:依文件頁數收費(可能免費或需付費)
💡 實務技巧:若收到 483 表格,建議同步申請 EIR,以了解 FDA 的完整評估意見。
警告信(Warning Letter):正式違規通知
什麼是警告信?
According to FDA 警告信官方資料庫{:target=”_blank”},警告信是 FDA 發出的正式法規違規通知,表示設施存在嚴重的不合規問題,若未改善將面臨法律行動。
核心特性:
- 正式性:由 FDA 地區辦公室主管或總部官員簽發
- 公開性:所有警告信會公開於 FDA 官網,可被公眾查詢
- mandatory:必須在 15 個工作天內書面回覆改善計畫
警告信的常見違規類型
- CGMP 違規:未遵守現行良好作業規範(Current Good Manufacturing Practice)
- FSMA 違規:未建立預防性控制計畫、HACCP 系統缺失
- 摻假或標示不實:產品含有未申報成分、標籤誤導消費者
- 未註冊或未通報:設施未完成 FDA 註冊、產品未通報
收到警告信的嚴重後果
- 進口扣留:所有產品可能被 FDA 自動扣留(Import Alert)
- Product Recall:FDA 可要求強制召回已上市產品
- Legal proceedings:可能面臨民事或刑事訴訟
- 聲譽損害:警告信公開於官網,影響品牌形象
圖 3: FDA 檢查報告應對流程圖
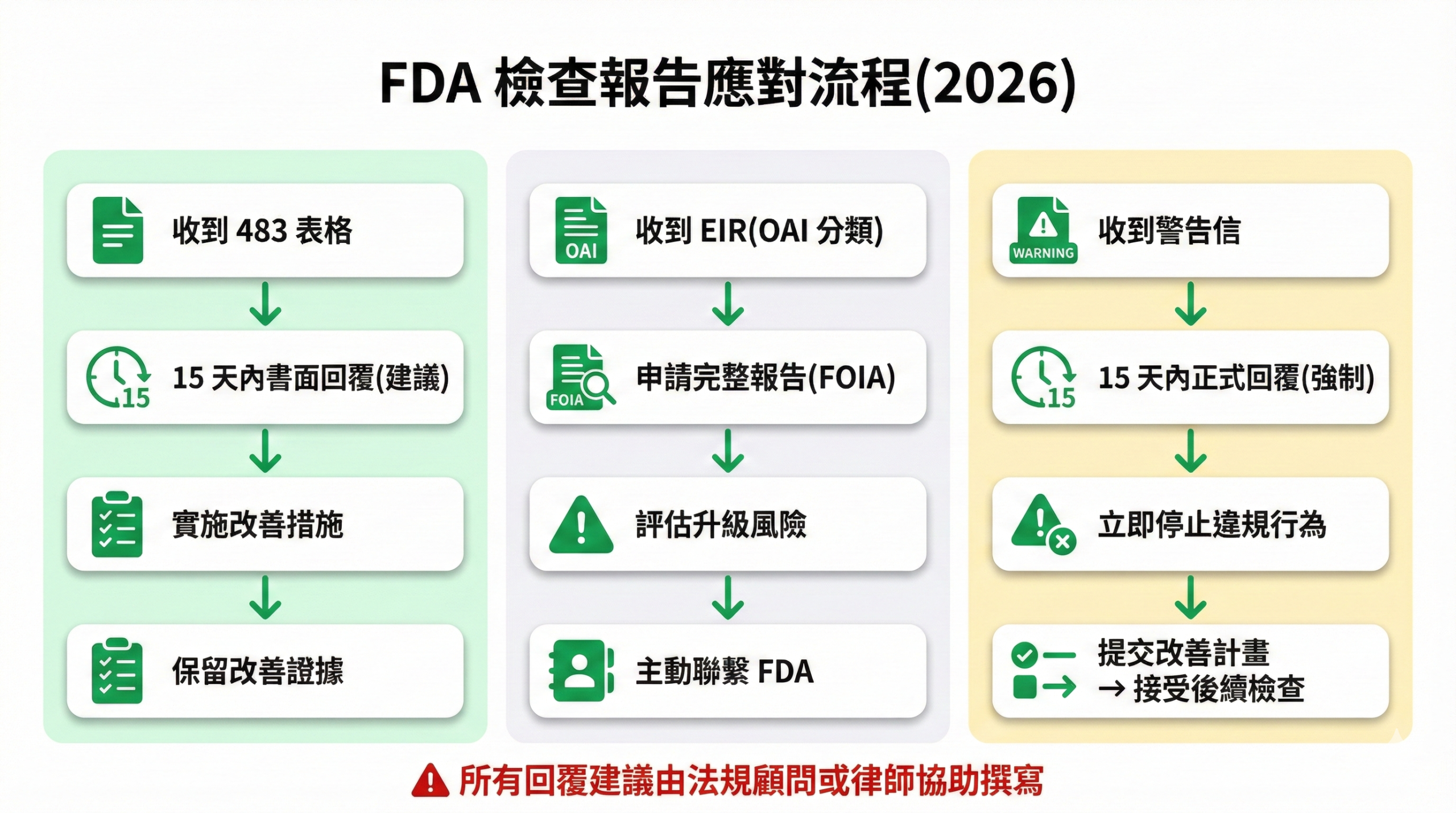
需要特別注意的 4 個重點
1. 483 表格不等於警告信,但可能升級
Common Misconceptions:許多台灣業者以為收到 483 表格就代表嚴重違規,其實 483 只是初步通知。但若未妥善回應,FDA 可能在後續評估後升級為警告信。
2. EIR 分類決定後續行動
實務判斷:若 EIR 被分類為 OAI(Official Action Indicated),代表 FDA 認為需採取正式行動,此時應主動聯繫 FDA 了解具體疑慮,避免直接收到警告信。
3. 警告信回覆需專業協助
風險提醒:警告信的回覆內容會成為法律文件,強烈建議由熟悉 FDA 法規的律師或顧問協助撰寫,避免因用詞不當導致更嚴重後果。
4. 所有檢查報告都會影響風險評級
長期影響:即使成功回應 483 表格或警告信,FDA 仍會將此記錄納入設施的風險評級,可能導致未來檢查頻率增加或進口審查更嚴格The
若進一步關心 FDA 食品註冊的扣關、查驗與常見錯誤,可參考以下說明頁面,以釐清實務上的判斷重點。
👉 FDA 食品註冊風險解析|扣關、查驗與常見錯誤整理(2026)
https://greenoo.tw/fda-food-registration-fda-food-registration-risks-and-inspections/
Conclusion
- 483 表格:檢查中發現的可觀察缺失,建議 15 天內回覆,屬於初步通知
- EIR:完整檢查報告,供 FDA 內部評估,可透過 FOIA 申請取得
- 警告信:正式違規通知,必須 15 天內回覆,未改善將面臨法律行動
- 正確應對:所有檢查報告都應認真對待,書面回覆前建議諮詢專業顧問
- 預防為主:建立完善的食品安全計畫與內部稽核機制,降低檢查風險
若對 FDA 食品合規與檢查應對仍有疑問,歡迎參考 Green Circle Official Website 的專業顧問服務。
參考資料
本文內容基於以下 FDA 官方資料撰寫(截至 2026 年 1 月):
- U.S. Food and Drug Administration. “Inspection Guides.” FDA.gov, https://www.fda.gov/inspections-compliance-enforcement-and-criminal-investigations/inspection-guides
- U.S. Food and Drug Administration. “Investigations Operations Manual (IOM).” FDA.gov, https://www.fda.gov/inspections-compliance-enforcement-and-criminal-investigations/inspection-references/investigations-operations-manual
- U.S. Food and Drug Administration. “Warning Letters.” FDA.gov, https://www.fda.gov/inspections-compliance-enforcement-and-criminal-investigations/compliance-actions-and-activities/warning-letters
- Code of Federal Regulations Title 21, § 20.64. “Establishment Inspection Reports.” eCFR, https://www.ecfr.gov/current/title-21/section-20.64
註:FDA 法規可能更新,建議查閱最新官方文件或諮詢專業顧問。
