IOR 需要準備哪些文件?
According to FDA 進口程序規定,IOR(Importer of Record,進口紀錄商)在進口食品至美國時,必須準備三大類文件:FDA 合規文件、CBP 海關報關文件、FSVP 供應商驗證資料。缺少任何一類文件,都可能導致貨物扣關、額外檢驗或銷毀。
台灣食品業者常誤以為只需提供商業發票與裝箱單即可清關,實際上 FDA 與 CBP(美國海關與邊境保護局)要求的文件遠比想像複雜。特別是 2026 年 FSMA 法規全面實施後,FSVP(外國供應商驗證計畫)文件已成為進口商的強制義務。
本文將完整列出 IOR 必備文件清單,並提供可複製的 Checklist 與常見錯誤整理,幫助台灣業者避免進口風險。
為何 IOR 文件準備如此重要?
IOR 是美國海關認定的進口責任主體,負責確保進口貨物符合所有聯邦法規。依據 CFR Title 19 § 141.1,進口商必須在貨物抵達前或抵達時,向 CBP 提交完整的進口申報文件。
若文件不齊全或資訊錯誤,CBP 有權拒絕放行貨物,甚至依據 FSMA 進口商驗證規則,要求額外檢驗或銷毀不合規產品。對台灣食品業者而言,文件準備不足可能導致:
- 貨物扣關:平均增加 7-14 天清關時間
- Additional costs:倉儲費、檢驗費、代理費用累積
- 客戶信任流失:交期延誤影響商業關係
- 進口警示風險:重複違規可能被列入 FDA 進口警示清單
若尚未建立對 FDA 食品註冊制度的整體理解,建議先從完整總覽入手,有助於後續判斷不同情境與執行差異。
👉 FDA 食品註冊完整指南|台灣食品出口美國必讀(2026 最新)
https://greenoo.tw/fda-food-registration/
IOR 必備文件完整清單
第一類:FDA 合規文件
| 文件名稱 | 用途說明 | 取得方式 | Points of Attention |
|---|---|---|---|
| FDA 食品設施註冊編號(FFR) | 證明製造設施已註冊 FDA | 透過 FDA FFR 系統線上申請 | 每兩年需更新一次 |
| 產品成分清單 | 供 FDA 審查產品合規性 | 由製造商提供完整配方 | 必須列出所有添加物 |
| 標籤樣本 | 確認符合 FDA 標籤規定 | 提供實際使用的產品標籤 | 須含營養標示與過敏原聲明 |
| 食品安全計畫(若適用) | 證明符合 FSMA 預防性控制規則 | 由製造商建立 HARPC 計畫 | 加工食品通常需要此文件 |
第二類:CBP 海關報關文件
| 文件名稱 | 用途說明 | 取得方式 | Points of Attention |
|---|---|---|---|
| 商業發票(Commercial Invoice) | 記錄交易金額與產品資訊 | 由出口商開立 | 須含 HS Code 與產品描述 |
| 裝箱單(Packing List) | 列出貨物數量與包裝方式 | 由出口商提供 | 須與實際貨物一致 |
| 提單(Bill of Lading) | 證明貨物運輸權利 | 由貨運公司開立 | 海運用 B/L,空運用 AWB |
| 進口商識別號碼 | 證明 IOR 身份 | 向 CBP 申請 EIN 或使用 SSN | 台灣業者需透過美國代理人取得 |
第三類:FSVP 供應商驗證資料
According to FSMA FSVP 規則,進口商必須建立外國供應商驗證計畫,並保留以下文件:
| 文件名稱 | 用途說明 | 取得方式 | Points of Attention |
|---|---|---|---|
| 供應商評估報告 | 證明供應商具備食品安全能力 | 進口商自行評估或委託第三方 | 須每年更新 |
| 危害分析文件 | 識別產品可能的食品安全風險 | 由進口商或供應商提供 | 須涵蓋生物、化學、物理危害 |
| 驗證活動紀錄 | 證明已執行供應商驗證 | 保留檢驗報告、稽核紀錄等 | 須保存至少 2 年 |
| 合格證明文件 | 證明產品符合美國食品安全標準 | 由供應商提供 COA 或檢驗報告 | 須由認可實驗室出具 |
圖 2:IOR 文件準備完整流程圖
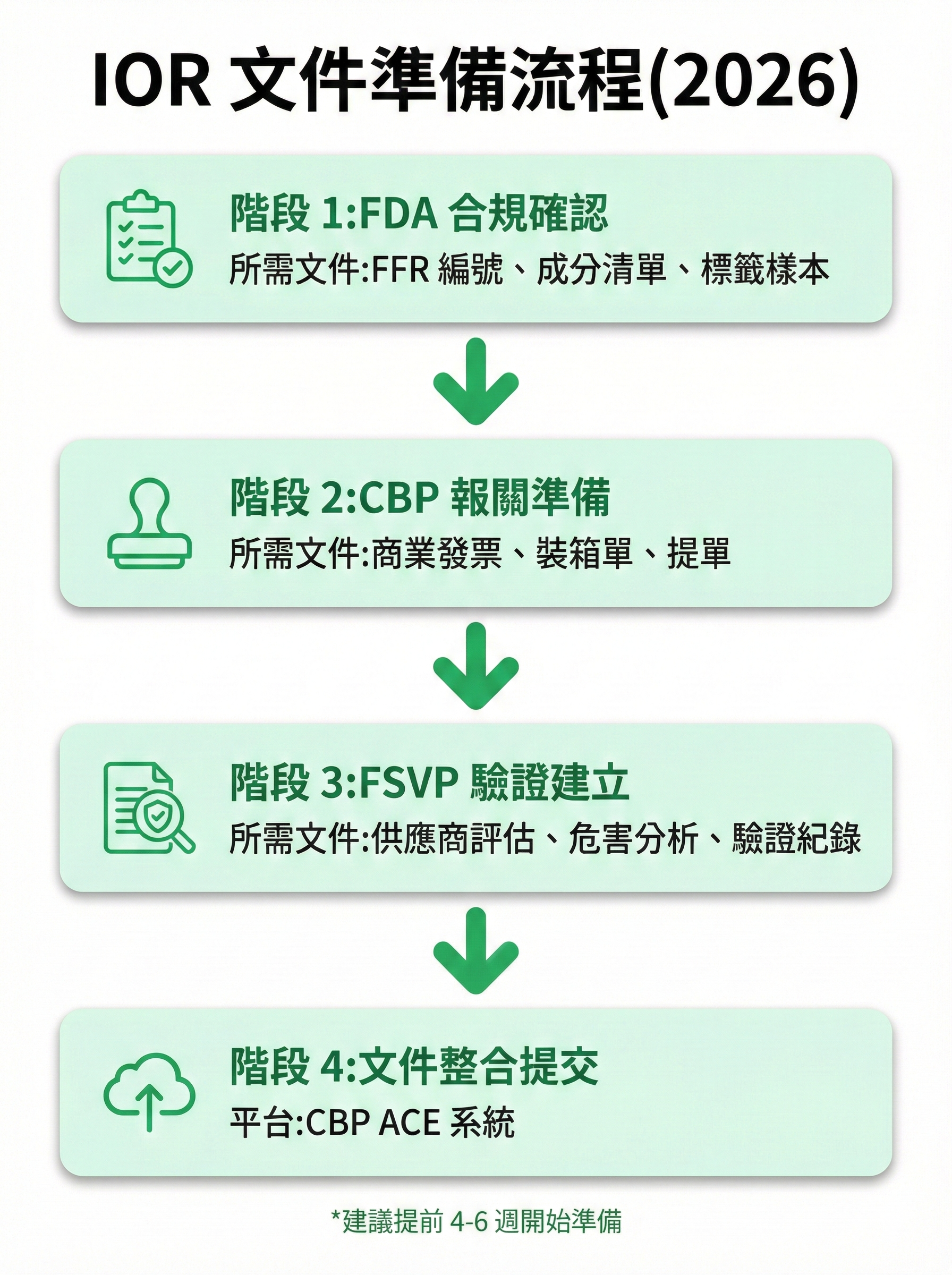
可複製的 IOR 文件檢核表
以下 Checklist 可直接複製使用,建議在出貨前 4-6 週開始逐項確認:
FDA 合規文件檢核
- 已取得 FDA 食品設施註冊編號(FFR)
- 已準備完整產品成分清單(含添加物)
- 已提供符合 FDA 規定的標籤樣本
- 已建立食品安全計畫(若為加工食品)
- 已確認產品無 FDA 進口警示限制
CBP 報關文件檢核
- 已取得商業發票(含正確 HS Code)
- 已準備裝箱單(與實際貨物一致)
- 已取得提單或空運提單
- 已確認 IOR 識別號碼(EIN 或 SSN)
- 已確認美國代理人資訊
FSVP 驗證文件檢核
- 已完成供應商評估(含食品安全能力確認)
- 已建立危害分析文件
- 已保留驗證活動紀錄(稽核或檢驗報告)
- 已取得合格證明文件(COA 或檢驗報告)
- 已確認 FSVP 代理人(若委外執行)
其他必要文件檢核
- 已準備原產地證明(若需要)
- 已取得有機認證(若為有機產品)
- 已確認產品保險文件
- 已備妥緊急聯絡人資訊
台灣業者常見的 5 大文件錯誤
錯誤 1:FFR 編號過期未更新
情境:台灣工廠 2 年前完成 FDA 設施註冊,但未定期更新,導致進口時 FFR 編號失效。
Proper Practice:FDA 設施註冊每兩年需更新一次(偶數年 10 月 1 日至 12 月 31 日)。建議設定提醒,避免過期。
錯誤 2:成分清單不完整
情境:僅列出主要成分,未標註食品添加物或加工助劑,導致 FDA 要求補件。
Proper Practice:依據 CFR Title 21 § 101.4所有成分必須完整列出,包含微量添加物。
錯誤 3:FSVP 文件缺失
情境:進口商未建立 FSVP,僅依賴供應商提供的檢驗報告,被 CBP 要求補充驗證計畫。
Proper Practice:進口商必須自行建立 FSVP,包含供應商評估、危害分析與驗證活動,不可僅依賴供應商文件。
錯誤 4:標籤不符合 FDA 規定
情境:產品標籤未標註過敏原或營養標示格式錯誤,導致貨物扣關。
Proper Practice:標籤必須符合 FDA Food Labeling Guidance包含營養成分表、過敏原聲明與製造商資訊。
錯誤 5:商業發票資訊錯誤
情境:HS Code 誤填或產品描述不清,導致 CBP 要求重新申報,延誤清關時間。
Proper Practice:商業發票必須使用正確的 HS Code(可透過 美國國際貿易委員會 HTS 查詢系統確認),並提供詳細的產品描述。
圖 3:IOR 文件常見錯誤檢核表

需要特別注意的 3 個進階議題
議題 1:低風險食品是否需要 FSVP?
並非所有食品都需要完整的 FSVP 文件。依據 FDA 規定,低風險食品(如罐頭、果汁等)可適用簡化版 FSVP,但仍需保留供應商評估與危害分析文件。建議諮詢專業顧問判定產品適用範圍。
議題 2:使用第三方物流是否影響 IOR 責任?
即使委託第三方物流(3PL)處理進口,IOR 的法律責任仍由進口商承擔。台灣業者需確保 3PL 具備 FDA 與 CBP 合規經驗,並保留完整的文件備份。
議題 3:文件保存期限與查核風險
根據 FDA 規定,FSVP 相關文件須保存至少 2 年,CBP 報關文件須保存 5 年。若 FDA 或 CBP 執行查核,進口商必須在 24 小時內提供文件,否則可能面臨罰款或進口限制。
若進一步關心 FDA 食品註冊的風險與查驗機制,可參考以下說明頁面,以釐清實務上的判斷重點。
👉 FDA 食品註冊風險解析|扣關、查驗與常見錯誤整理(2026)
https://greenoo.tw/fda-food-registration-fda-food-registration-risks-and-inspections/
Conclusion
IOR 進口商必須準備三大類文件:FDA 合規文件(FFR 編號、成分清單、標籤)、CBP 報關文件(商業發票、裝箱單、提單)、FSVP 供應商驗證資料(供應商評估、危害分析、驗證紀錄)。台灣業者常見錯誤包含 FFR 過期、成分清單不完整、FSVP 缺失、標籤不合規、HS Code 錯誤。
建議使用本文提供的 Checklist 逐項確認,並在出貨前 4-6 週開始準備文件,避免進口扣關風險。若對 FDA 食品進口文件仍有疑問,歡迎參考 Green Circle Official Website 的專業顧問服務。
參考資料
本文內容基於以下 FDA 官方資料撰寫(截至 2026 年 1 月):
- U.S. Food and Drug Administration. “Import Basics.” FDA.gov, https://www.fda.gov/industry/import-basics
- U.S. Food and Drug Administration. “FSMA Final Rule on Foreign Supplier Verification Programs (FSVP) for Importers of Food for Humans and Animals.” FDA.gov, https://www.fda.gov/food/food-safety-modernization-act-fsma/fsma-final-rule-foreign-supplier-verification-programs-fsvp-importers-food-humans-and-animals
- Code of Federal Regulations Title 19, § 141.1. “Entry of Merchandise.” eCFR, https://www.ecfr.gov/current/title-19/section-141.1
- Code of Federal Regulations Title 21, § 101.4. “Food; Designation of Ingredients.” eCFR, https://www.ecfr.gov/current/title-21/section-101.4
- U.S. Food and Drug Administration. “Food Labeling & Nutrition.” FDA.gov, https://www.fda.gov/food/food-labeling-nutrition
註:FDA 法規可能更新,建議查閱最新官方文件或諮詢專業顧問。
