FDA 稽查文件是什麼?為何台灣業者需要了解?
根據 FDA 稽查程序規定當 FDA 對食品設施進行稽查時,會依據發現的缺失嚴重程度,核發不同類型的官方文件。FDA 483 表格(Form 483)、稽查報告(Establishment Inspection Report, EIR)與警告信(Warning Letter)是三種最常見的稽查結果文件,直接影響台灣食品業者的出口資格與市場准入。
理解這三種文件的差異與應對策略,能有效降低扣關風險、避免罰款,並維護品牌聲譽。特別是在 FSMA(食品安全現代化法案)實施後,FDA 稽查頻率與嚴格度大幅提升,台灣業者必須建立完整的合規應對機制。
若尚未建立對 FDA 食品註冊制度的整體理解,建議先從完整總覽入手,有助於後續判斷不同情境與執行差異。
👉 FDA 食品註冊完整指南|台灣食品出口美國必讀(2026 最新)
https://greenoo.tw/fda-food-registration/
FDA 483 表格:稽查缺失的正式通知
什麼是 FDA 483 表格?
依據 CFR Title 21 § 20.64,FDA 483 表格是稽查官在現場稽查結束時,向設施負責人提供的書面觀察報告,列出所有發現的潛在違規事項或需改善的缺失。
核心特徵:
- 現場即時核發(稽查結束前)
- 列出具體觀察到的缺失(非最終判定)
- 設施有 15 個工作日回應期限
- 不代表 FDA 最終執法行動
常見 483 表格缺失類型
| 缺失類型 | 具體範例 | 風險等級 |
|---|---|---|
| 文件記錄不完整 | 食品安全計畫未定期更新 | 中等 |
| 環境衛生問題 | 生產區域發現蟲害跡象 | 高 |
| 人員訓練不足 | 員工未接受過敏原管理訓練 | 中等 |
| 設備維護缺失 | 溫度監控設備未校正 | 高 |
| 標籤不符規定 | 過敏原標示遺漏或錯誤 | 高 |
收到 483 表格後的正確應對
步驟 1: 立即組成內部應對小組(1-2 天內)
- 指定專責人員統籌回應
- 召集品保、生產、法務部門
- 建立缺失改善時程表
步驟 2: 詳細分析每項缺失(3-5 天內)
- 確認缺失的根本原因
- 評估改善所需資源與時間
- 優先處理高風險項目
步驟 3: 提交書面回應給 FDA(15 個工作日內)
- 說明每項缺失的改善措施
- 提供改善完成時程
- 附上相關證明文件(照片、SOP 修訂版等)
⚠️ 重要提醒: 未在期限內回應或回應不完整,可能導致 FDA 升級為警告信或進口警示,嚴重影響出口業務。
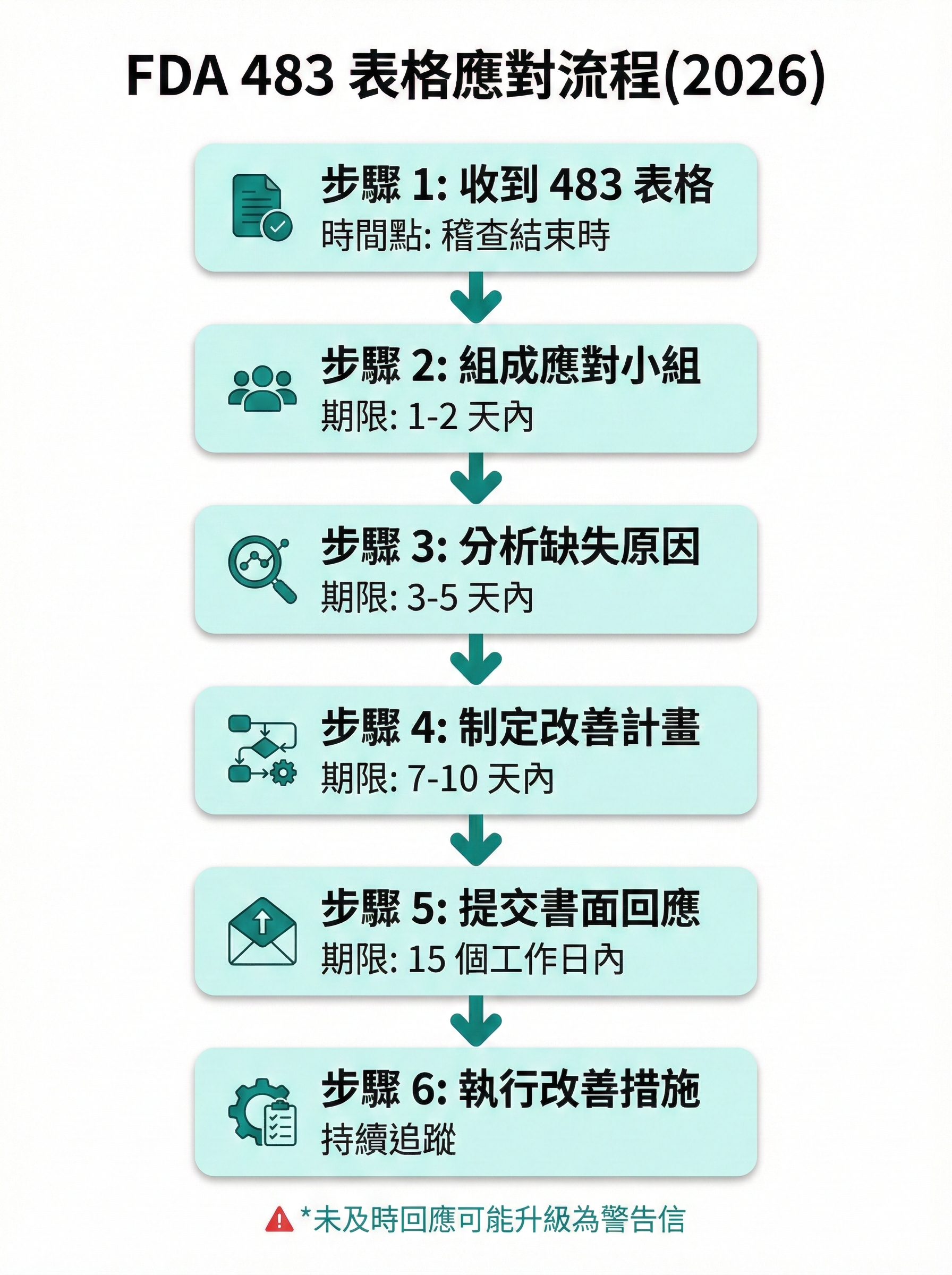
圖 2: FDA 483 表格應對流程圖
EIR 稽查報告:FDA 的完整評估結論
什麼是 EIR?
稽查報告(Establishment Inspection Report, EIR)是 FDA 稽查官完成現場稽查後,提交給 FDA 總部的完整評估文件,記錄稽查過程、發現的問題與初步結論。
EIR 與 483 表格的差異:
| 項目 | FDA 483 表格 | EIR 稽查報告 |
|---|---|---|
| 核發時間 | 稽查結束時現場交付 | 稽查後數週至數月 |
| 接收對象 | 設施負責人 | FDA 內部使用 |
| 內容範圍 | 僅列出觀察到的缺失 | 完整稽查過程與評估 |
| 公開性 | 可透過 FOIA 申請取得 | 可透過 FOIA 申請取得 |
| 後續影響 | 需在 15 天內回應 | 作為執法行動依據 |
EIR 的三種分類結果
根據 FDA 稽查分類系統EIR 會給予以下三種分類:
NAI(No Action Indicated)無需採取行動
- 未發現違規或僅有輕微缺失
- 不影響產品安全與合規性
- 無需後續執法行動
VAI(Voluntary Action Indicated)建議自願改善
- 發現需改善的缺失,但未達嚴重程度
- 設施應自行改善,但 FDA 不會強制執法
- 可能進行後續追蹤稽查
OAI(Official Action Indicated)需採取官方行動
- 發現嚴重違規,需 FDA 正式介入
- 可能導致警告信、進口警示或產品扣押
- 必須立即改善並提供證明
警告信:FDA 的正式執法通知
什麼是警告信?
依據 FDA 警告信政策警告信(Warning Letter)是 FDA 針對嚴重違規行為發出的正式執法文件,要求設施立即改善,否則將面臨更嚴厲的法律行動。
警告信的嚴重後果:
- 產品可能被扣押或召回
- 進口貨物遭海關扣留
- 面臨民事或刑事罰款
- 公司名稱公開於 FDA 網站
- 嚴重損害品牌聲譽
收到警告信後的應對策略
立即行動(收到後 15 天內):
- 停止相關違規行為
- 聘請專業法規顧問協助
- 提交詳細的改善計畫(CAPA, Corrective and Preventive Action)
- 說明已採取的立即措施
長期改善(後續 30-90 天):
- 全面檢視設施合規狀態
- 更新 SOP 與員工訓練
- 建立內部稽核機制
- 定期向 FDA 報告改善進度
💡 實務技巧: 警告信回應品質直接影響 FDA 後續執法決定,建議尋求專業顧問協助撰寫,避免因回應不當導致更嚴重後果。
圖 3: FDA 稽查文件嚴重程度對照表

如何預防 FDA 稽查缺失?
建立完善的內部稽核機制:
- 每季進行自我稽核,模擬 FDA 稽查流程
- 建立缺失追蹤系統,確保改善措施落實
- 定期更新 SOP,符合最新 FDA 法規
加強員工訓練與文件管理:
- 所有員工必須接受 GMP(良好作業規範)訓練
- 建立完整的文件記錄系統(電子化優先)
- 確保過敏原管理與標籤合規
尋求專業顧問協助:
- 定期諮詢 FDA 法規專家
- 在稽查前進行預審(Pre-Audit)
- 建立緊急應對 SOP
若進一步關心 FDA 食品註冊的風險與查驗細節,可參考以下說明頁面,以釐清實務上的判斷重點。
👉 FDA 食品註冊風險解析|扣關、查驗與常見錯誤整理(2026)
https://greenoo.tw/fda-food-registration-fda-food-registration-risks-and-inspections/
總結
- FDA 483 表格是稽查現場核發的缺失通知,必須在 15 個工作日內提交書面回應
- EIR 稽查報告是 FDA 內部評估文件,分為 NAI、VAI、OAI 三種等級
- 警告信是最嚴重的執法文件,可能導致扣關、罰款與產品召回
- 收到任何 FDA 稽查文件都應立即組成應對小組,並尋求專業顧問協助
- 預防勝於治療:建立完善的內部稽核機制與員工訓練,降低稽查風險
若對 FDA 食品合規仍有疑問,歡迎參考 綠圈圈官網 的專業顧問服務。
參考資料
本文內容基於以下 FDA 官方資料撰寫(截至 2026 年 1 月):
- U.S. Food and Drug Administration. “Inspection Guides.” FDA.gov, https://www.fda.gov/inspections-compliance-enforcement-and-criminal-investigations/inspection-guides
- Code of Federal Regulations Title 21, § 20.64. “Establishment Inspection Report.” eCFR, https://www.ecfr.gov/current/title-21/section-20.64
- U.S. Food and Drug Administration. “Inspection Classification Database.” FDA.gov, https://www.fda.gov/inspections-compliance-enforcement-and-criminal-investigations/inspection-classification-database
- U.S. Food and Drug Administration. “Warning Letters.” FDA.gov, https://www.fda.gov/inspections-compliance-enforcement-and-criminal-investigations/compliance-actions-and-activities/warning-letters
註:FDA 法規可能更新,建議查閱最新官方文件或諮詢專業顧問。
