FDA 快速通道認定的「快」,指的不是核准速度
根據 FDA 快速通道計畫官方說明{:target=”_blank”},快速通道認定(Fast Track Designation)的核心目的是加速開發與審查流程,而非縮短最終核准時間。實際上,從提交快速通道申請到取得認定,通常需要 60 天;而從認定到最終產品核准,則可能需要 數個月至數年,取決於臨床試驗進度、資料完整性與疾病類別。
台灣醫藥業者常見的三大誤解包括:
- 誤解一: 快速通道 = 快速核准(實際上是加速審查,非保證核准)
- 誤解二: 申請後立即生效(實際需 60 天審查期)
- 誤解三: 適用所有藥品(僅限嚴重疾病且有未滿足醫療需求)
若對 FDA 快速通道認定的整體制度與申請資格仍不清楚,建議先從完整的 FDA 藥品審查制度理解起,有助於後續判斷不同加速路徑的適用性與時程規劃。
為何台灣醫藥業者需要了解快速通道時程?
FDA 快速通道認定是美國為加速治療嚴重疾病藥品上市而設立的制度,但「加速」的範圍與實際時程常被誤解。台灣醫藥業者若計劃透過快速通道進入美國市場,必須理解:
- 時程規劃: 快速通道並非「申請後立即加速」,而是需經過正式審查與認定程序
- 資源配置: 認定後可享有的審查優勢(如滾動審查、優先審查),需提前準備相應資料
- 投資決策: 快速通道認定不保證最終核准,時程預估影響臨床試驗與商業化規劃
根據 FDASIA(FDA 安全與創新法案){:target=”_blank”},快速通道計畫於 2012 年正式法制化,旨在縮短嚴重疾病治療藥品的開發時程,但實際執行時程仍受多重因素影響。
若尚未建立對 FDA 食品註冊制度的整體理解,建議先從完整總覽入手,有助於後續判斷不同情境與執行差異。
👉 FDA 食品註冊完整指南|台灣食品出口美國必讀(2026 最新)
https://greenoo.tw/fda-food-registration/
FDA 快速通道認定的完整時程拆解
階段一:申請前準備(3-6 個月)
在正式提交快速通道申請前,業者需完成以下準備:
- 疾病嚴重性評估: 確認目標疾病符合 FDA 定義的「嚴重疾病」(如癌症、罕見疾病、危及生命的感染症)
- 未滿足醫療需求證明: 準備現有治療選項不足的科學證據
- 初步臨床數據: 至少需有第一期臨床試驗數據,顯示潛在療效
- 開發計畫書: 詳細說明後續臨床試驗設計與時程
依據 CFR Title 21 § 312.81{:target=”_blank”},快速通道申請必須包含「藥品用於治療嚴重疾病且有潛力滿足未滿足醫療需求」的充分證據。
階段二:快速通道申請提交與審查(60 天)
正式提交快速通道認定申請後,FDA 的標準審查時程為 60 天:
- 提交方式: 透過 IND(Investigational New Drug Application)或 NDA(New Drug Application)程序提交
- 審查重點: FDA 評估疾病嚴重性、未滿足醫療需求、初步臨床數據
- 溝通機制: 審查期間 FDA 可能要求補充資料或召開會議澄清疑問
實務注意: 60 天為「標準時程」,若資料不完整或需補件,審查時間可能延長至 90-120 天。
圖 2: FDA 快速通道認定時程流程圖
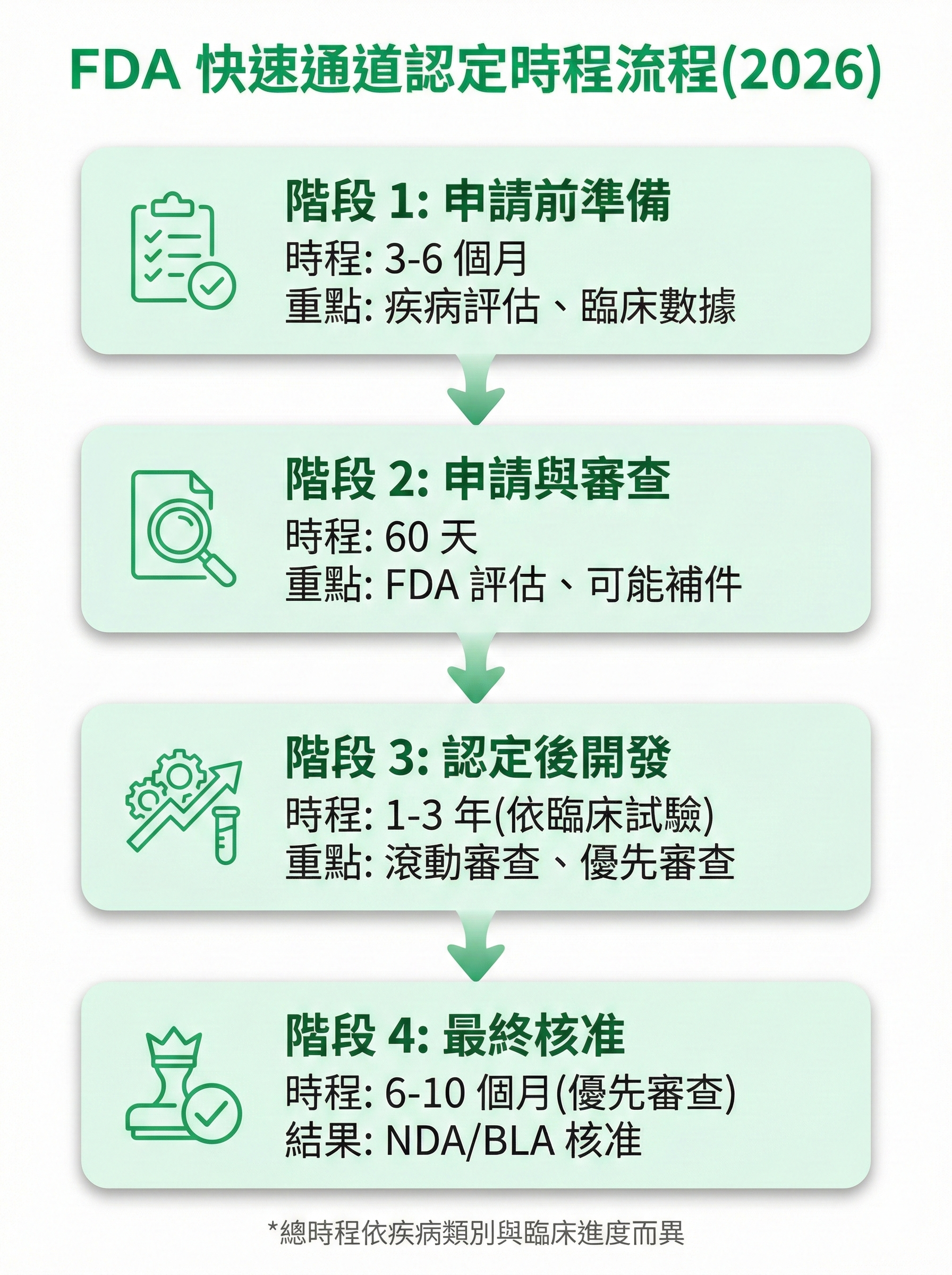
階段三:認定後的加速開發(1-3 年)
取得快速通道認定後,業者可享有以下審查優勢,但開發時程仍取決於臨床試驗進度:
滾動審查(Rolling Review):
- 允許分批提交 NDA/BLA 資料,無需等待所有數據完成
- 可縮短最終審查時程約 2-4 個月
優先審查資格:
- 若符合條件,可申請優先審查(Priority Review),審查時程從標準 10 個月縮短至 6 個月
頻繁溝通:
- FDA 提供更密集的會議與指導,協助解決開發過程中的技術問題
實務案例: 某罕見癌症藥品取得快速通道認定後,透過滾動審查提交第三期臨床數據,最終從認定到核准歷時 18 個月,較傳統路徑縮短約 12 個月。
階段四:最終核准(6-10 個月)
完成所有臨床試驗並提交完整 NDA/BLA 後,FDA 的審查時程為:
- 優先審查: 6 個月(適用快速通道認定藥品)
- 標準審查: 10 個月(若未取得優先審查資格)
重要提醒: 快速通道認定不保證最終核准,FDA 仍會嚴格審查安全性與療效數據。
快速通道認定的實際時程影響因素
快速通道認定的「快」受以下因素影響:
| 影響因素 | 說明 | 時程影響 |
|---|---|---|
| 疾病類別 | 罕見疾病、癌症優先程度較高 | 可縮短 3-6 個月 |
| 臨床數據完整性 | 第三期臨床試驗數據是否充分 | 不完整可能延長 6-12 個月 |
| FDA 溝通頻率 | 主動與 FDA 溝通可減少補件次數 | 可避免 2-4 個月延誤 |
| 滾動審查執行 | 是否善用滾動審查分批提交 | 可縮短 2-4 個月 |
| 優先審查資格 | 是否同時取得優先審查 | 可縮短 4 個月 |
圖 3: FDA 快速通道認定時程影響因素檢核表

需要特別注意的 3 個時程誤區
誤區一:快速通道 = 快速核准
快速通道認定僅是「加速審查流程」,並非「保證快速核准」。FDA 仍會嚴格審查安全性與療效,若數據不足,核准時程不會縮短。
誤區二:申請後立即享有優勢
快速通道申請需經 60 天審查期,且認定後的滾動審查、優先審查仍需符合額外條件,並非自動享有。
誤區三:所有藥品都能申請
快速通道僅適用於「治療嚴重疾病且有未滿足醫療需求」的藥品,一般慢性病或生活品質改善藥品不符合資格。
總結
- FDA 快速通道認定的「快」指加速審查流程,非保證快速核准
- 從申請到認定需 60 天,從認定到核准需 1-3 年(依臨床進度)
- 取得認定後可享滾動審查、優先審查等優勢,但需符合額外條件
- 時程受疾病類別、臨床數據完整性、FDA 溝通頻率等因素影響
- 台灣醫藥業者應提前規劃時程,避免誤解「快速通道 = 快速核准」
若對 FDA 藥品審查制度與快速通道認定仍有疑問,歡迎參考 綠圈圈官網 的專業顧問服務。
參考資料
本文內容基於以下 FDA 官方資料撰寫(截至 2026 年 1 月):
- U.S. Food and Drug Administration. “Fast Track, Breakthrough Therapy, Accelerated Approval, Priority Review.” FDA.gov, https://www.fda.gov/patients/fast-track-breakthrough-therapy-accelerated-approval-priority-review/fast-track
- U.S. Food and Drug Administration. “Food and Drug Administration Safety and Innovation Act (FDASIA).” FDA.gov, https://www.fda.gov/regulatory-information/selected-amendments-fdc-act/food-and-drug-administration-safety-and-innovation-act-fdasia
- Code of Federal Regulations Title 21, § 312.81. “Scope.” eCFR, https://www.ecfr.gov/current/title-21/section-312.81
註:FDA 法規可能更新,建議查閱最新官方文件或諮詢專業顧問。
