【2026最新】FDA認證流程詳解:臺灣品牌出海美國市場必讀指南
你知道嗎?超過65%的首次申請FDA認證的臺灣品牌經營者因資料準備不足而被退件!本文將為您揭示完整FDA認證流程,助您一次通過審核。
FDA 認證是什麼?台灣品牌為何需要了解?
FDA 認證並非單一程序,而是依產品類型適用不同的合規要求。根據 FDA 官方定義{:target=”_blank”},美國食品藥物管理局(FDA)負責監管食品、藥品、化妝品、醫療器材等產品的安全性,台灣品牌若要進入美國市場,必須先判定產品屬性,再依循對應的註冊或申報流程。
實務上,台灣業者常誤以為「FDA 認證」是統一的申請程序,但實際情況是:食品需進行設施註冊(Facility Registration)、化妝品採自願性註冊(Voluntary Cosmetic Registration Program, VCRP)、醫療器材則依風險等級分為 510(k)、PMA 等不同申請途徑。若未正確判定產品類型,可能導致申請方向錯誤或遭海關扣留。
若尚未建立對 FDA 食品註冊制度的整體理解,建議先從完整總覽入手,有助於後續判斷不同情境與執行差異。
👉 FDA 食品註冊完整指南|台灣食品出口美國必讀(2026 最新)
https://greenoo.tw/fda-food-registration/
FDA 認證流程核心步驟
依據 FDA 產品分類系統{:target=”_blank”},台灣品牌出海美國需完成以下核心判定與申請流程:
步驟一:產品類型判定(最關鍵)
首要任務是確認產品屬於哪一類受 FDA 監管的商品。常見分類包括:
- 食品(Food): 供人類或動物食用的產品,包含膳食補充劑、飲料、包裝食品
- 化妝品(Cosmetics): 用於清潔、美化或改變外觀的產品,如保養品、彩妝
- 醫療器材(Medical Devices): 用於診斷、治療或預防疾病的設備或工具
- 藥品(Drugs): 具有治療、預防疾病功效的產品
⚠️ 常見誤區: 許多保健食品在美國可能被歸類為「膳食補充劑(Dietary Supplements)」,屬於食品類別而非藥品,但若宣稱療效則可能被視為未經核准的新藥。
圖 2: FDA 產品類型判定流程圖
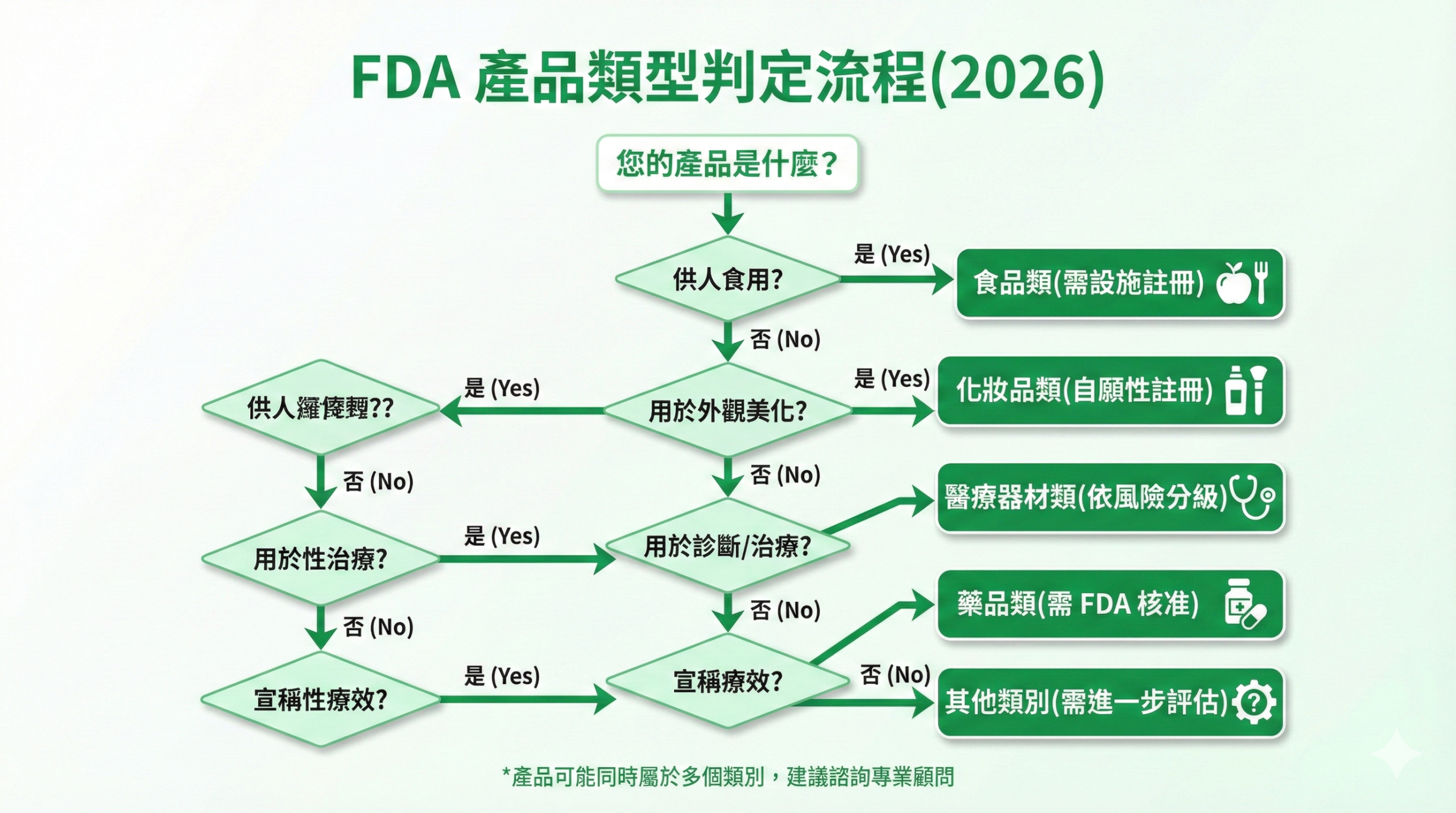
步驟二:確認適用的法規要求
不同產品類型適用不同的 FDA 法規:
| 產品類型 | 主要法規 | 註冊/申報要求 | 預估時程 |
|---|---|---|---|
| 食品 | FSMA 法案{:target=”_blank”} | 設施註冊(FFR)、FSVP(進口商) | 即時-4 週 |
| 化妝品 | CFR Title 21 Part 700-740 | VCRP 自願性註冊 | 即時 |
| 醫療器材 Class I | CFR Title 21 Part 800-1299 | 多數豁免 510(k) | 1-3 個月 |
| 醫療器材 Class II | 同上 | 需提交 510(k) | 3-6 個月 |
| 醫療器材 Class III | 同上 | 需提交 PMA | 1-2 年 |
💡 實務技巧: 食品類產品若同時在 Amazon 等平台銷售,需額外準備 FDA 設施註冊編號(FFR Number)供平台審核使用。
步驟三:指定美國代理人(僅食品類必須)
依據 CFR Title 21 § 1.33{:target=”_blank”},所有在美國境外的食品設施必須指定一位美國代理人(US Agent),作為 FDA 與設施之間的聯絡窗口。代理人必須:
- 實際位於美國境內(具美國地址與聯絡方式)
- 能以英語溝通並協助處理緊急事件
- 可為個人或企業,但不得為郵政信箱
⚠️ 常見錯誤: 許多台灣業者誤以為美國代理人需具備律師或顧問資格,實際上任何符合條件的美國居民或公司皆可擔任,但建議選擇熟悉 FDA 法規的專業服務商。
步驟四:完成線上註冊或申報
根據產品類型,前往對應的 FDA 系統完成註冊:
- 食品: FDA 食品設施註冊系統(FFR){:target=”_blank”}
- 化妝品: VCRP 自願性註冊系統{:target=”_blank”}
- 醫療器材: FURLS 統一註冊系統{:target=”_blank”}
註冊時需準備的基本資料包括:
- 設施完整地址與聯絡資訊
- 產品類別與製程描述
- 美國代理人資訊(食品類)
- DUNS 號碼(部分情況需要)
步驟五:維持合規與定期更新
FDA 註冊並非一次性作業,不同類型產品有不同的更新週期:
- 食品設施註冊: 每兩年更新一次(偶數年 10/1-12/31)
- 化妝品 VCRP: 產品配方或設施資訊變更時需更新
- 醫療器材: 每年 6 月及資訊變更時需更新
此外,食品設施若適用 FSMA 預防性控制規則,還需建立並維護書面食品安全計畫,定期進行內部稽核。
圖 3: FDA 認證流程時程與檢核表
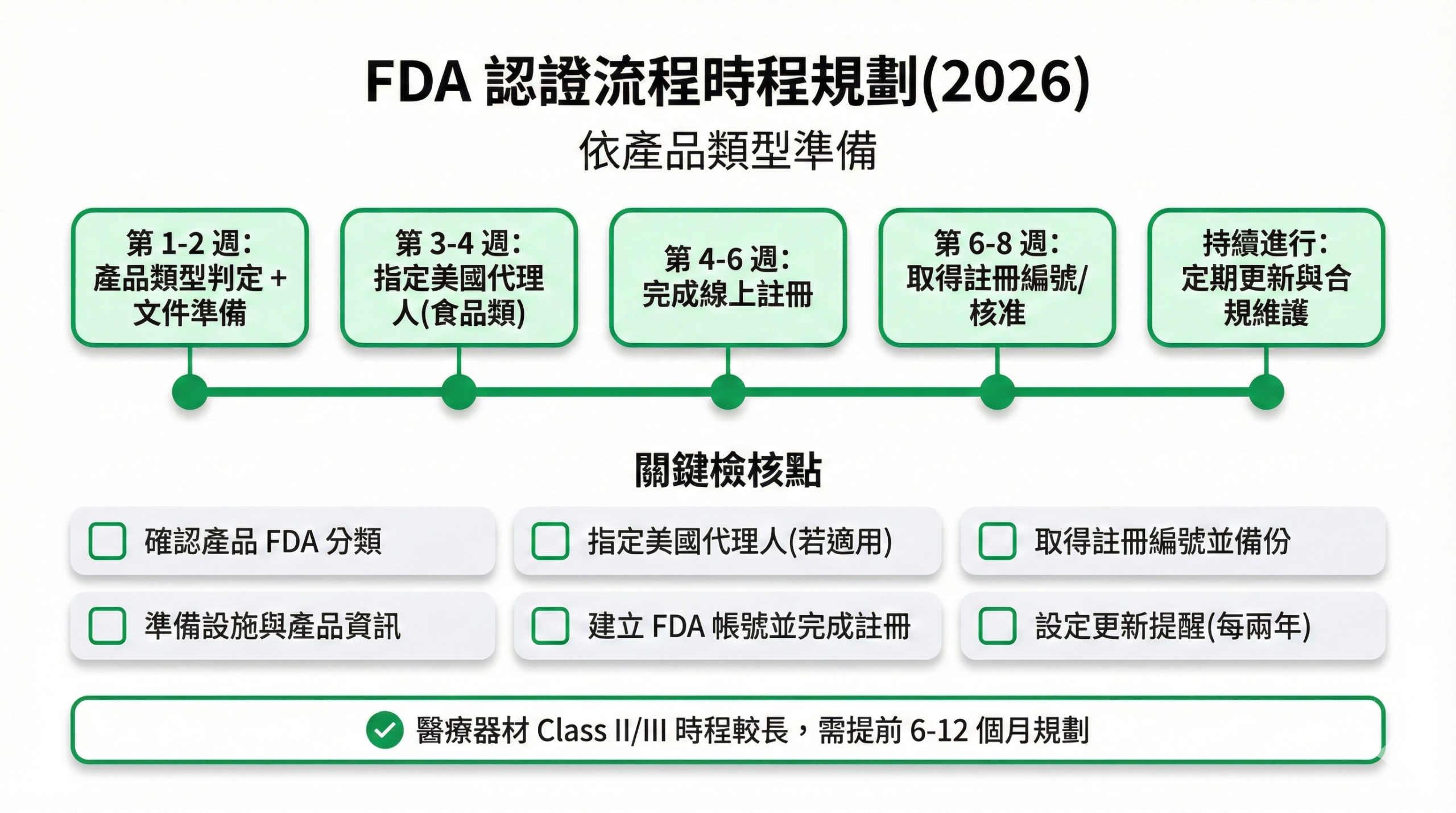
需要特別注意的 3 個重點
1. 產品可能同時屬於多個類別
某些產品可能同時符合多個 FDA 監管類別。例如,含藥化妝品(Drug-Cosmetic)既需符合化妝品法規,也需遵守藥品規範。台灣業者應審慎評估產品宣稱與成分,避免誤判類別導致合規問題。
2. Amazon 等平台有額外審核要求
若進一步關心 Amazon 平台對 FDA 食品註冊的審核要求,可參考以下說明頁面,以釐清實務上的判斷重點。
👉 Amazon 為何要求 FDA 食品註冊?平台審核規則完整解析(2026)
https://greenoo.tw/fda-food-registration-amazon-fda-food-registration-requirements/
3. 標籤與宣稱需符合 FDA 規定
無論產品類型為何,所有在美國銷售的產品標籤必須符合 CFR Title 21 標籤規範{:target=”_blank”},包含:
- 成分列表(Ingredients List)
- 營養標示(Nutrition Facts,食品類)
- 警語與使用說明
- 製造商或進口商資訊
❌ 常見誤區: 台灣業者常直接使用中文標籤翻譯,但 FDA 對於過敏原標示、營養成分格式、字體大小等皆有明確要求,需重新設計符合美國規範的英文標籤。
總結
台灣品牌出海美國市場,FDA 認證流程的核心在於:
- 正確判定產品類型(食品、化妝品、醫療器材、藥品)
- 依循對應法規完成註冊或申報(FFR、VCRP、510(k)、PMA 等)
- 指定美國代理人(食品類必須,其他類別視情況)
- 定期更新維持合規(食品每兩年、醫療器材每年)
- 確保標籤與宣稱符合 FDA 規範(避免誤導或違規)
建議台灣品牌在產品開發階段即納入 FDA 合規考量,提前 3-6 個月規劃認證流程,避免因法規問題延誤上市時程。
若對 FDA 認證流程仍有疑問,歡迎參考 綠圈圈官網 的專業顧問服務。
參考資料
本文內容基於以下 FDA 官方資料撰寫(截至 2026 年 1 月):
- U.S. Food and Drug Administration. “What Does FDA Regulate?” FDA.gov, https://www.fda.gov/about-fda/fda-basics/what-does-fda-regulate
- U.S. Food and Drug Administration. “Food Safety Modernization Act (FSMA).” FDA.gov, https://www.fda.gov/food/food-safety-modernization-act-fsma
- U.S. Food and Drug Administration. “How to Determine If Your Product Is a Medical Device.” FDA.gov, https://www.fda.gov/medical-devices/classify-your-medical-device/how-determine-if-your-product-medical-device
- Code of Federal Regulations Title 21, Part 1.33. “What is a U.S. agent?” eCFR, https://www.ecfr.gov/current/title-21/section-1.33
- U.S. Food and Drug Administration. “Food Facility Registration.” FDA.gov, https://www.fda.gov/food/food-facility-registration
註:FDA 法規可能更新,建議查閱最新官方文件或諮詢專業顧問。
