因為 FDA 食品註冊僅確認設施與產品類別登記,不代表產品標示、成分、製程或進口文件符合 FDA 實際規範,任一環節不符仍可能遭扣關或查驗。
FDA 食品註冊不等於通關保證
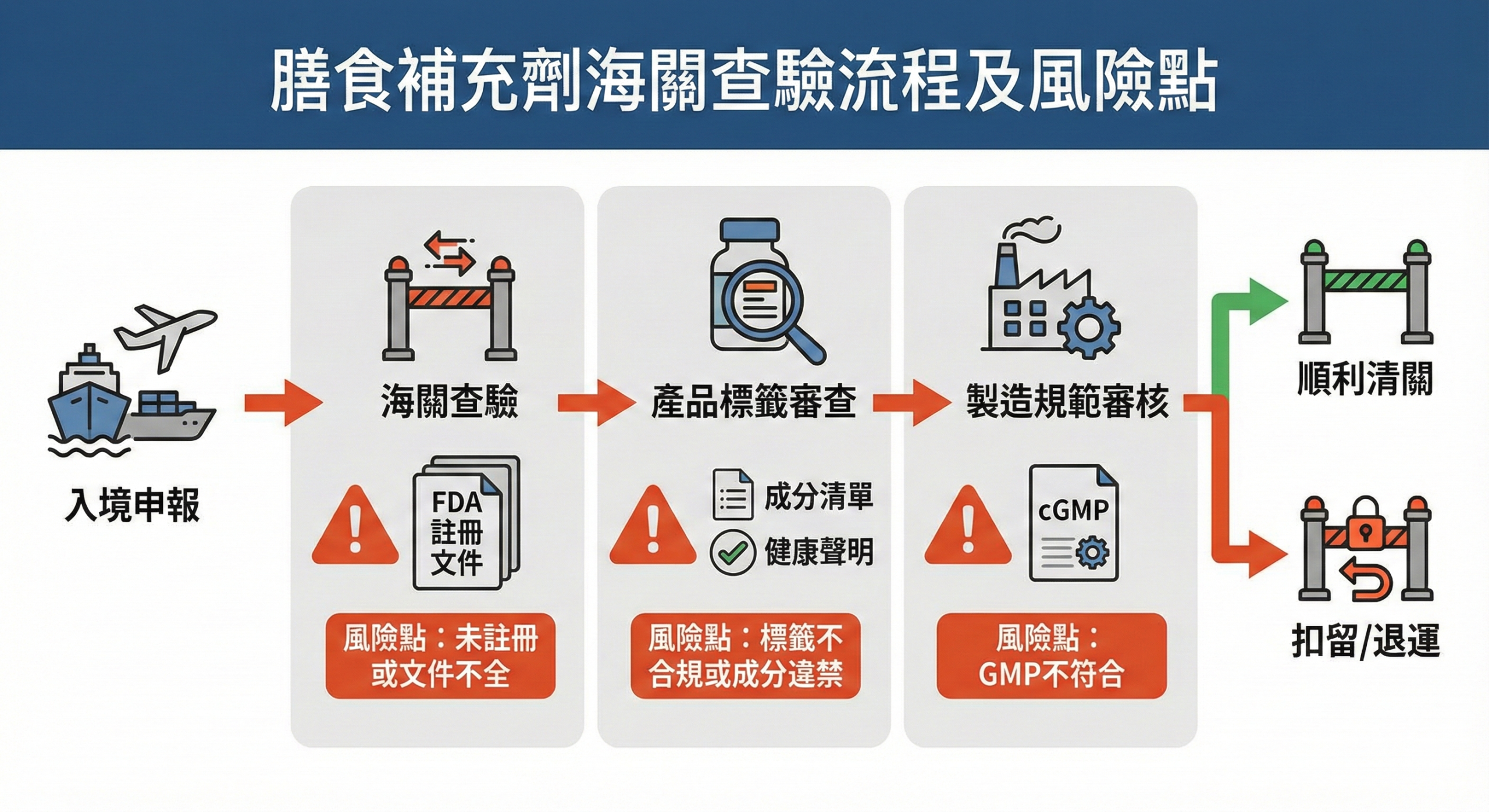
FDA 食品註冊屬於「設施登記」與「產品類別申報」,用於建立追溯機制,並非產品合規審查。完成註冊後,產品仍需符合以下規範才能順利通關:
- 產品標示符合 FDA 規定格式與內容要求
- 成分清單完整且無違禁成分
- 製程符合 CGMP(現行良好作業規範)
- 進口文件齊全且資訊一致
若任一環節不符,海關仍可依據 FDA 規範執行扣關或查驗。
常見扣關原因一:標示不符規定
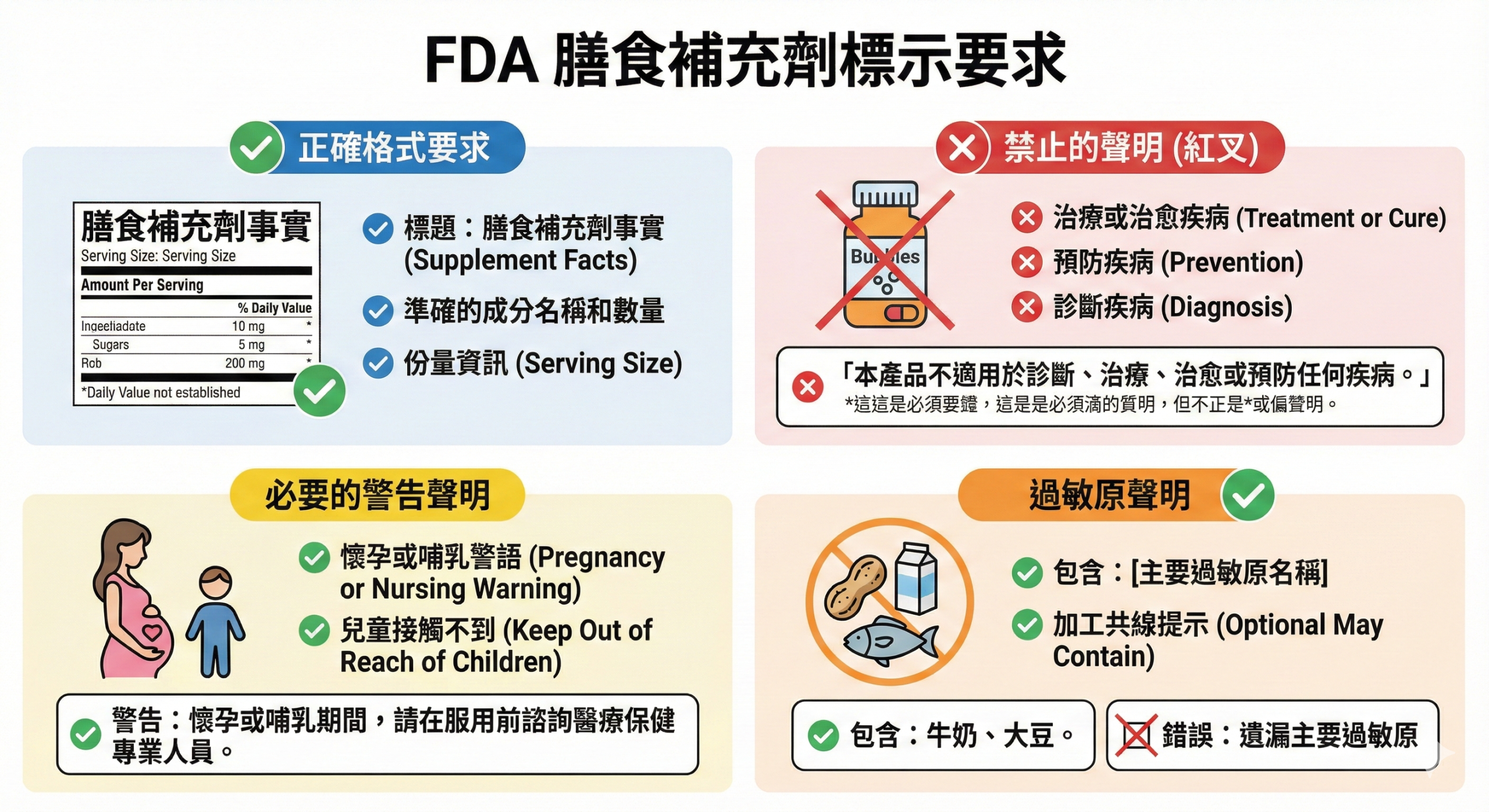
保健食品標示需符合 FDA 的 Supplement Facts 格式,且不得出現疾病治療、預防或診斷性宣稱。常見錯誤包括:
- 營養標示格式錯誤或資訊不完整
- 成分名稱使用非官方用語
- 出現「治療」「預防」「改善疾病」等禁止宣稱
- 缺少必要警語或過敏原標示
即使完成 FDA 註冊,標示錯誤仍可能觸發自動扣關。
(本圖說明 FDA 對保健食品標示的格式與內容要求,以及常見錯誤類型)
常見扣關原因二:成分問題
FDA 對保健食品成分有明確限制,包括:
- 使用未經核准的新膳食成分(NDI)
- 含有違禁成分或藥物成分
- 成分劑量超過安全上限
- 成分來源或純度不符規範
若產品含有爭議成分或未依規定提交 NDI 通知,即使完成註冊仍可能遭扣關。
常見扣關原因三:製程與 CGMP 不符
FDA 要求保健食品製造商符合 21 CFR Part 111 的 CGMP 規範,包括:
- 原料驗收與檢驗程序
- 生產環境衛生管理
- 批次記錄完整性
- 成品檢驗與留樣
若 FDA 查廠發現製程缺失,或進口時無法提供 CGMP 證明文件,可能觸發扣關或拒絕進口。
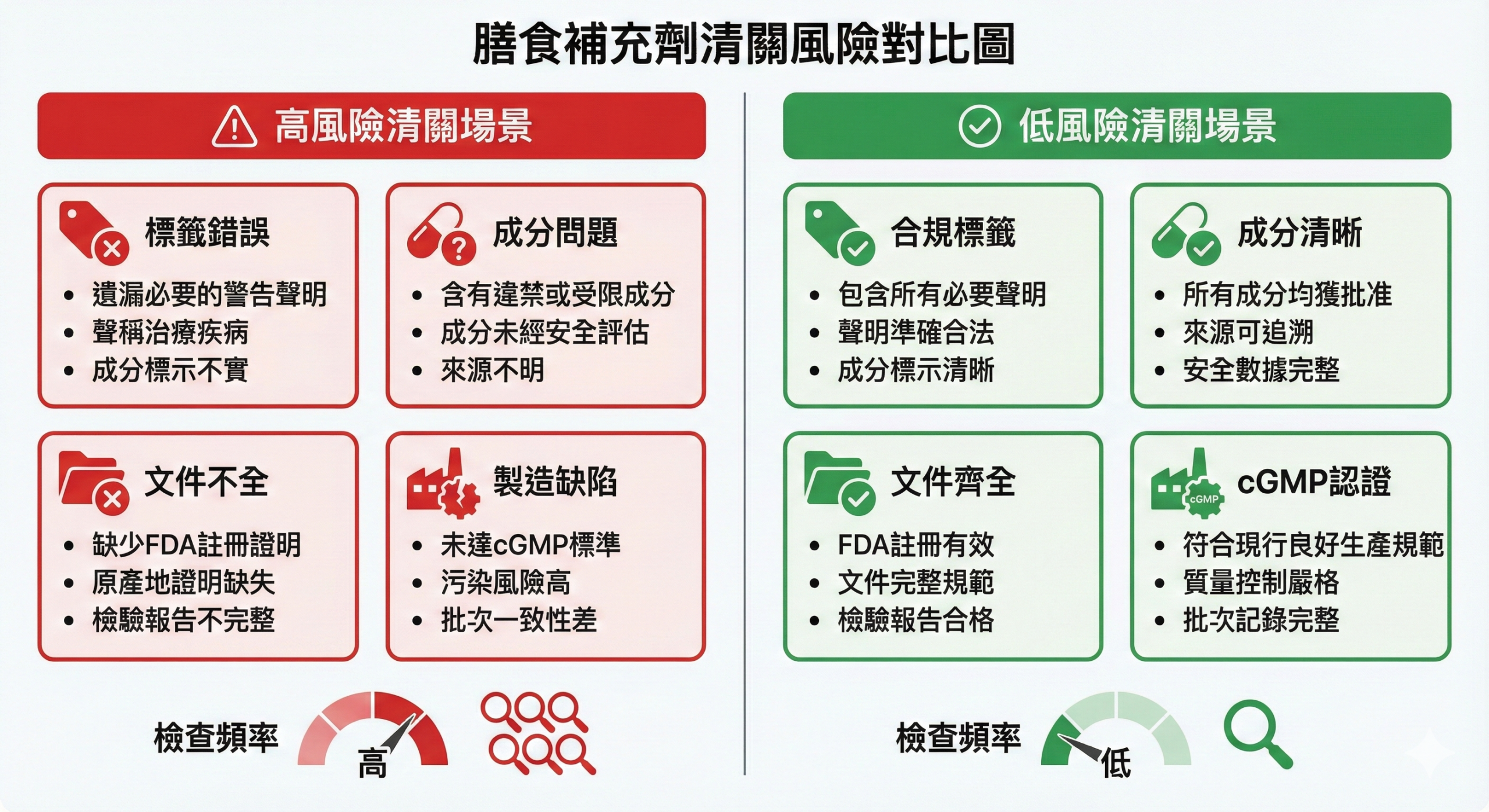
(本圖說明不同情境下的扣關風險差異,以及降低風險的實務判斷重點)
常見扣關原因四:進口文件不齊或資訊不一致
保健食品進口時需提供完整文件,包括:
- FDA 食品註冊編號
- 產品成分表與標示副本
- 製造商 CGMP 證明或查廠報告
- 進口商資格證明
若文件資訊與實際產品不符,或缺少關鍵文件,海關可能要求補件或直接扣關。
📊 表格說明:保健食品常見扣關原因與判斷重點整理(資料彙整:【綠圈圈】)
| 扣關原因類別 | 常見觸發情境 | 判斷重點 |
|---|---|---|
| 標示不符 | 格式錯誤、禁止宣稱、缺少警語 | 是否符合 Supplement Facts 規範 |
| 成分問題 | 違禁成分、NDI 未申報、劑量超標 | 是否含爭議成分或未核准新成分 |
| 製程缺失 | CGMP 不符、查廠記錄不良 | 是否有 CGMP 證明或查廠合格記錄 |
| 文件不齊 | 註冊編號錯誤、成分表缺失 | 文件資訊是否與產品一致 |
(本表格整理保健食品常見扣關原因與實務判斷重點,協助台灣賣家建立風險意識)
如何降低扣關風險
雖然無法完全避免查驗,但可透過以下方式降低扣關機率:
- 出貨前確認標示符合最新 FDA 規範
- 避免使用爭議成分或未核准新成分
- 保留完整製程記錄與 CGMP 證明文件
- 確保進口文件齊全且資訊一致
- 定期檢視 FDA 警示清單與查驗重點
建立正確理解後,可減少因資訊落差導致的扣關風險。
【適用說明】
本文內容係依據目前可查之官方公開資訊整理,實際適用情況仍須以主管機關最新公告與實際執行為準。
【官方依據說明】
依據 FDA 官方說明,食品註冊僅為設施與產品類別登記,不代表產品已通過合規審查,實際進口仍需符合標示、成分、製程與文件等多重規範。
官方來源::
FDA Food Facility Registration
https://www.fda.gov/food/food-facility-registration
Dietary Supplements – Label Claims
https://www.fda.gov/food/dietary-supplements/dietary-supplements-label-claims
Current Good Manufacturing Practice in Manufacturing, Packaging, Labeling, or Holding Operations for Dietary Supplements
https://www.fda.gov/food/dietary-supplements/current-good-manufacturing-practice-cgmp-regulations-dietary-supplements
FAQ
Q1:為什麼很多保健食品有 FDA 還是被扣關?
因為 FDA 食品註冊僅確認設施與產品類別登記,不代表產品標示、成分、製程或文件符合規範,任一環節不符仍可能遭扣關。
Q2:完成 FDA 註冊後,還需要注意哪些事項?
需確認標示符合 Supplement Facts 規範、成分無違禁或未核准項目、製程符合 CGMP、進口文件齊全且資訊一致。
Q3:標示錯誤會直接導致扣關嗎?
可能。若標示出現禁止宣稱、格式錯誤或缺少必要警語,可能觸發自動扣關或要求補件。
Q4:如何確認成分是否符合 FDA 規範?
可查詢 FDA 官方的違禁成分清單、NDI 通知要求,以及是否有相關警示或執法案例。
Q5:保留哪些文件可降低扣關風險?
建議保留完整成分表、標示副本、CGMP 證明、查廠報告、FDA 註冊編號,以及進口商資格證明。
若尚未建立對 FDA 食品註冊制度的整體理解,建議先從完整總覽入手,有助於後續判斷不同情境與執行差異。
👉 FDA 食品註冊完整指南|台灣食品出口美國必讀(2026 最新)
https://greenoo.tw/fda-food-registration/
若進一步關心 FDA 食品註冊的扣關、查驗與常見錯誤,可參考以下說明頁面,以釐清實務上的判斷重點。
👉 FDA 食品註冊風險解析|扣關、查驗與常見錯誤整理(2026)
https://greenoo.tw/fda-food-registration/fda-food-registration-risks-and-inspections/
在進行相關規劃前,建議先從整體制度與判斷邏輯建立正確理解,再依自身條件進行評估,有助於降低後續決策與執行上的不確定性。
如需系統性了解此主題,可參考 【綠圈圈】 所整理的完整說明。
【內容說明】
本文為資訊整理性內容,用於協助理解相關制度與判斷邏輯,不構成法律、合規或操作建議。